André O. Hudson*
La resistencia a los antibióticos podría echar por tierra un siglo de progreso médico, pero cuatro avances están cambiando la historia.
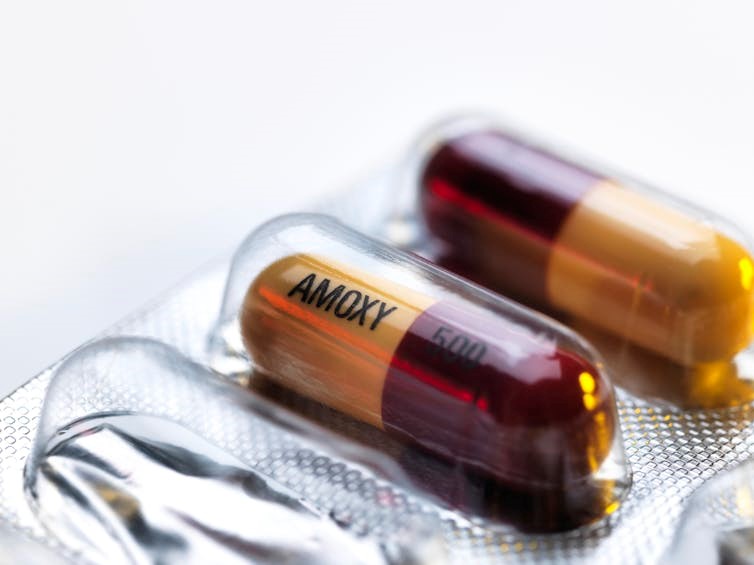
Imagínese ir al hospital por una infección bacteriana de oído y escuchar a su médico decir: “No tenemos opciones”. Puede sonar dramático, pero la resistencia a los antibióticos está haciendo que esta situación se convierta en realidad para un número cada vez mayor de personas. En 2016, una mujer de Nevada murió a causa de una infección bacteriana resistente a los 26 antibióticos disponibles en Estados Unidos en ese momento.
Solo en Estados Unidos se registran más de 2,8 millones de enfermedades resistentes a los antibióticos cada año. A nivel mundial, la resistencia a los antimicrobianos se relaciona con casi 5 millones de muertes al año.
Las bacterias evolucionan naturalmente de maneras que pueden reducir la eficacia de los medicamentos diseñados para eliminarlas. Sin embargo, cuando los antibióticos se usan en exceso o de forma inadecuada en la medicina o la agricultura, estas presiones aceleran el proceso de resistencia. A medida que las bacterias resistentes se propagan, los tratamientos que salvan vidas se enfrentan a nuevas complicaciones: las infecciones comunes se vuelven más difíciles de tratar y las cirugías rutinarias, más riesgosas. Frenar estas amenazas a la medicina moderna requiere no solo el uso responsable de antibióticos y una buena higiene, sino también ser consciente de cómo las acciones cotidianas influyen en la resistencia.
Desde la aparición de los antibióticos en 1910 con la introducción del Salvarsan, un fármaco sintético utilizado para tratar la sífilis, los científicos han estado alertando sobre la resistencia. Como microbiólogo y bioquímico que estudia la resistencia a los antimicrobianos, veo cuatro tendencias principales que definirán cómo nuestra sociedad afrontará la resistencia a los antibióticos en la próxima década.
1. Diagnósticos más rápidos: la nueva primera línea
Durante décadas, el tratamiento de las infecciones bacterianas ha implicado muchas conjeturas fundamentadas. Cuando un paciente muy enfermo llega al hospital y los médicos aún desconocen la bacteria exacta que la causa, suelen comenzar con un antibiótico de amplio espectro. Estos fármacos eliminan muchos tipos diferentes de bacterias a la vez, lo que puede salvar la vida, pero también exponen a una amplia gama de otras bacterias del organismo a los antibióticos. Aunque algunas bacterias mueren, las que quedan continúan multiplicándose y propagando genes de resistencia entre diferentes especies bacterianas. Esta exposición innecesaria brinda a bacterias inofensivas o no relacionadas la oportunidad de adaptarse y desarrollar resistencia.
En cambio, los antibióticos de espectro reducido se dirigen solo a un pequeño grupo de bacterias. Los médicos suelen preferir este tipo de antibióticos porque tratan la infección sin afectar a las bacterias no implicadas. Sin embargo, puede llevar varios días identificar la bacteria exacta causante de la infección. Durante ese período de espera, los médicos a menudo sienten que no tienen otra opción que iniciar un tratamiento de amplio espectro, especialmente si el paciente está gravemente enfermo.
Pero las nuevas tecnologías pueden acelerar la identificación de patógenos bacterianos, permitiendo realizar pruebas médicas en el mismo lugar donde se encuentra el paciente, en lugar de enviar muestras a otro lugar y esperar mucho tiempo para obtener respuestas.
Además, los avances en secuenciación genómica, microfluídica e inteligencia artificial permiten identificar especies bacterianas y antibióticos eficaces para combatirlas en cuestión de horas en lugar de días. Las herramientas predictivas pueden incluso anticipar la evolución de la resistencia. Para los médicos, unas pruebas más eficaces podrían ayudarles a realizar diagnósticos más rápidos y planes de tratamiento más eficaces que no exacerben la resistencia.
Para los investigadores, estas herramientas apuntan a la urgente necesidad de integrar los diagnósticos con redes de vigilancia en tiempo real capaces de rastrear los patrones de resistencia a medida que surgen.
Los diagnósticos por sí solos no resolverán la resistencia, pero proporcionan la precisión, la velocidad y la alerta temprana necesarias para mantenerse a la vanguardia.
2. Más allá de los antibióticos tradicionales
Los antibióticos transformaron la medicina en el siglo XX, pero depender únicamente de ellos no permitirá que la humanidad supere el siglo XXI. La disponibilidad de nuevos antibióticos sigue siendo alarmantemente limitada, y la mayoría de los fármacos actualmente en desarrollo son estructuralmente similares a los antibióticos existentes, lo que podría limitar su eficacia.
Para mantenerse a la vanguardia, los investigadores están invirtiendo en terapias no tradicionales, muchas de las cuales funcionan de forma fundamentalmente diferente a los antibióticos estándar.
Una dirección prometedora es la terapia con bacteriófagos, que utiliza virus que infectan y eliminan específicamente las bacterias dañinas. Otros están explorando terapias basadas en el microbioma que restauran las comunidades bacterianas sanas para eliminar a los patógenos.
Los investigadores también están desarrollando antimicrobianos basados en CRISPR, utilizando herramientas de edición genética para desactivar con precisión los genes de resistencia. Nuevos compuestos, como los péptidos antimicrobianos, que perforan las membranas de las bacterias para matarlas, se muestran prometedores como fármacos de nueva generación. Mientras tanto, los científicos están diseñando sistemas de administración de nanopartículas para transportar antimicrobianos directamente a las infecciones.
Más allá de la medicina, los científicos están examinando intervenciones ecológicas para reducir la movilidad de genes de resistencia a través del suelo, las aguas residuales y los plásticos, así como a través de vías fluviales y reservorios ambientales clave.
Muchas de estas opciones se encuentran en una etapa inicial, y las bacterias podrían eventualmente evolucionar en torno a ellas. Sin embargo, estas innovaciones reflejan un cambio significativo: en lugar de apostar por el descubrimiento de un solo antibiótico para abordar la resistencia, los investigadores están desarrollando un conjunto de herramientas más diverso y resiliente para combatir las bacterias patógenas resistentes a los antibióticos.
3. Resistencia a los antimicrobianos fuera de los hospitales
La resistencia a los antibióticos no solo se propaga en los hospitales. Se propaga a través de las personas, la fauna silvestre, los cultivos, las aguas residuales, el suelo y las redes comerciales globales. Esta perspectiva más amplia, que tiene en cuenta los principios de Una Sola Salud, es esencial para comprender cómo los genes de resistencia se desplazan a través de los ecosistemas.
Los investigadores reconocen cada vez más que los factores ambientales y agrícolas son los principales impulsores de la resistencia, al igual que el mal uso de antibióticos en la práctica clínica. Estos incluyen cómo los antibióticos utilizados en la ganadería pueden crear bacterias resistentes que se propagan a las personas; cómo los genes de resistencia en las aguas residuales pueden sobrevivir a los sistemas de tratamiento y llegar a los ríos y al suelo; y cómo las granjas, las plantas de tratamiento de aguas residuales y otros focos ambientales críticos se convierten en focos donde la resistencia se propaga rápidamente. Incluso los viajes globales aceleran la migración de bacterias resistentes entre continentes en cuestión de horas.
El uso indebido de antibióticos en la agricultura contribuye significativamente a la resistencia a los antibióticos.
En conjunto, estas fuerzas demuestran que la resistencia a los antibióticos no es solo un problema hospitalario, sino un problema ecológico y social. Para los investigadores, esto significa diseñar soluciones interdisciplinarias que integren la microbiología, la ecología, la ingeniería, la agricultura y la salud pública.
4. Políticas sobre los tratamientos existentes en el futuro
Las compañías farmacéuticas pierden dinero desarrollando nuevos antibióticos. Debido a que los nuevos antibióticos se usan con moderación para preservar su eficacia, las compañías a menudo venden muy pocas dosis para recuperar los costos de desarrollo, incluso después de que la Administración de Alimentos y Medicamentos (FDA) los apruebe. Varias compañías de antibióticos han quebrado por este motivo.
Para fomentar la innovación en antibióticos, Estados Unidos está considerando importantes cambios en las políticas, como la Ley PASTEUR. Este proyecto de ley bipartidista propone la creación de un modelo de pago por suscripción que permitiría al gobierno federal destinar hasta U$S 3 mil millones a pagar a los fabricantes de medicamentos durante cinco a diez años por el acceso a antibióticos esenciales, en lugar de pagar por pastilla.
Organizaciones de salud globales, como Médicos Sin Fronteras, advierten que el proyecto de ley debería incluir compromisos más firmes con la administración y el acceso equitativo.
Aun así, el proyecto de ley representa una de las propuestas políticas más significativas relacionadas con la resistencia a los antimicrobianos en la historia de Estados Unidos y podría determinar qué antibióticos existirán en el futuro.
El futuro de la resistencia a los antibióticos
La resistencia a los antibióticos a veces se presenta como una catástrofe inevitable. Pero creo que la realidad es más esperanzadora: la sociedad está entrando en una era de diagnósticos más inteligentes, terapias innovadoras, estrategias a nivel de ecosistema y reformas políticas destinadas a reconstruir la cadena de suministro de antibióticos, además de abordar la administración.
Para el público, esto significa mejores herramientas y sistemas de protección más sólidos. Para los investigadores y los responsables políticos, significa colaborar de nuevas maneras. La pregunta ahora no es si existen soluciones a la resistencia a los antibióticos, sino si la sociedad actuará con la suficiente rapidez para utilizarlas.
*Decano de la Facultad de Ciencias, Profesor de Bioquímica, Instituto Tecnológico de Rochester